Rapporto sul mercato europeo degli studi clinici (2021-2031) per ambito, segmentazione, dinamiche e analisi competitiva
No. of Pages: 136 | Report Code: BMIRE00028989 | Category: Life Sciences
No. of Pages: 136 | Report Code: BMIRE00028989 | Category: Life Sciences
Si prevede che il mercato europeo degli studi clinici raggiungerà i 20.056,53 milioni di dollari entro il 2031, rispetto ai 12.286,73 milioni di dollari del 2023. Si stima che il mercato registrerà un CAGR del 6,3% dal 2023 al 2031.
Il mercato europeo degli studi clinici è stato segmentato in Regno Unito, Francia, Germania, Italia, Spagna, Polonia, Svizzera, Svezia, Danimarca, Belgio, Paesi Bassi e resto d'Europa. L'aumento del numero di attività di sperimentazione clinica per lo sviluppo di nuovi farmaci e il lancio di prodotti innovativi da parte delle aziende dovrebbe stimolare la crescita del mercato in Europa durante il periodo di previsione .
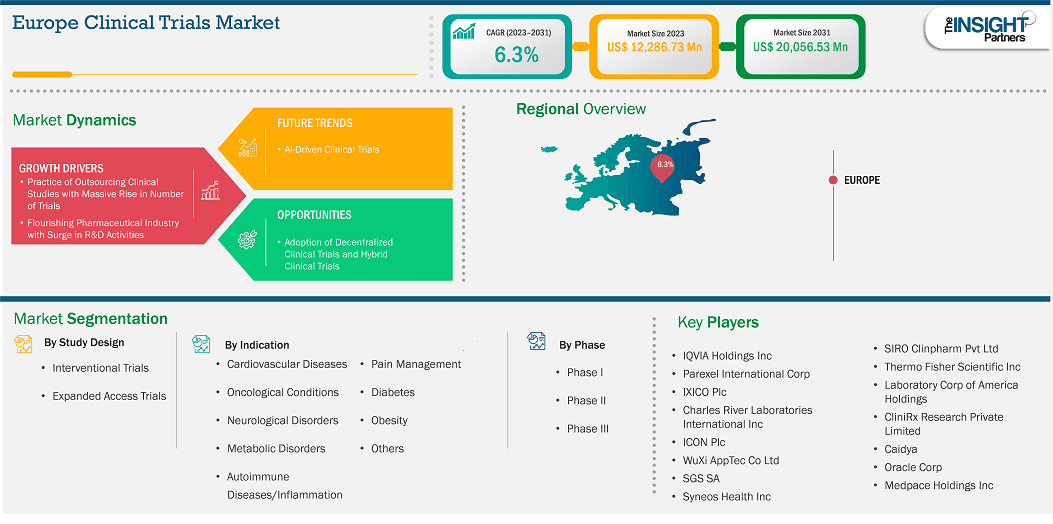
I segmenti chiave che hanno contribuito alla derivazione dell'analisi del mercato degli studi clinici in Europa sono la progettazione dello studio, le indicazioni e il tipo di fase.
I soggetti arruolati in studi clinici decentralizzati (DCT) non hanno bisogno di accedere frequentemente ai centri di sperimentazione ospedalieri. Nei DCT, le tecnologie digitali vengono utilizzate per consentire l'accesso dei pazienti alla ricerca clinica, la raccolta e il monitoraggio dei dati da remoto e la comunicazione tra ricercatori e partecipanti. Un approccio ibrido alla sperimentazione clinica combina attività svolte a domicilio e in loco, offrendo la migliore esperienza per il paziente e rispettando protocolli complessi, guadagnando terreno in diverse aree terapeutiche e fasi di sperimentazione. Inizialmente, l'adozione del DCT è stata ostacolata da sfide quali la privacy dei pazienti, la sicurezza dei dati, le barriere normative e la complessità dei protocolli. Tuttavia, la pandemia di COVID-19 ha costretto gli sponsor degli studi clinici ad adottare tecniche cliniche decentralizzate e ibride per lo sviluppo di farmaci, poiché gli studi in presenza non erano fattibili durante questa crisi sanitaria. Con le restrizioni imposte agli spostamenti, l'unico modo per raccogliere dati e proseguire gli studi era lavorare da remoto e sfruttare al meglio le tecnologie per accelerare i processi. Secondo i dati forniti da McKinsey, circa il 70% dei potenziali partecipanti agli studi clinici si allontana dai centri di sperimentazione. Pertanto, la decentralizzazione amplia l'accesso alla sperimentazione per raggiungere un numero maggiore di soggetti, costituito potenzialmente da un pool di pazienti più diversificato.
Gli studi clinici ibridi consentono agli sponsor di integrare strategicamente elementi DCT nei disegni di studio. Questi modelli di studio offrono una flessibilità senza precedenti; pertanto, sempre più aziende stanno mostrando interesse per gli studi ibridi, ridefinendo il panorama del settore. Secondo ObvioHealth, la FDA aveva in programma di presentare protocolli a supporto dell'uso dei metodi DCT nel 2023 per migliorare la credibilità della futura ricerca clinica. Pertanto, si prevede che la crescente attenzione all'utilizzo di studi clinici decentralizzati e ibridi rispetto ai metodi di sperimentazione clinica tradizionali offrirà opportunità redditizie per il mercato degli studi clinici durante il periodo di previsione.
Suddiviso per Paese, il mercato europeo degli studi clinici comprende Regno Unito, Germania, Francia, Spagna, Italia, Polonia, Svizzera, Svezia, Danimarca, Belgio, Paesi Bassi e il resto d'Europa. La Germania deteneva la quota maggiore nel 2023.
Secondo Clinical Trials Arena, la Germania ha ospitato circa il 3,9% del totale degli studi clinici condotti a livello globale nel 2021. Inoltre, nel Paese vi è un ampio bacino di pazienti e un'elevata domanda di assistenza sanitaria di qualità. Sono stati istituiti centri di coordinamento per gli studi clinici nell'ambito di un nuovo programma di finanziamento del Ministero Federale dell'Istruzione e della Ricerca per promuovere la ricerca clinica accademica. Gli studi clinici in Germania sono approvati dall'Istituto Federale per i Farmaci e i Dispositivi Medici o dal Paul-Ehrlich Institute, a seconda del prodotto da studiare. Pertanto, i processi di approvazione degli studi clinici in Germania sono standardizzati, affidabili, trasparenti e approvati per tempi di avvio degli studi relativamente brevi. Inoltre, le principali CRO in Germania forniscono diversi servizi per gli studi clinici. Sofpromed gestisce gli studi clinici in Germania e in altri Stati membri dell'UE. Offre una gamma completa di servizi CRO per aziende farmaceutiche e biotecnologiche. Allo stesso modo, CONET GmbH, con sede a Mannheim, in Germania, offre servizi di gestione di sperimentazioni cliniche, da piccoli studi pilota a grandi sperimentazioni cliniche multicentriche internazionali per tutte le fasi (1–4), comprese le sperimentazioni cliniche pediatriche e le sperimentazioni sui dispositivi medici, secondo le direttive UE.
| Attributo del report | Dettagli |
|---|---|
| Dimensioni del mercato nel 2023 | 12.286,73 milioni di dollari USA |
| Dimensioni del mercato entro il 2031 | 20.056,53 milioni di dollari USA |
| CAGR globale (2023 - 2031) | 6,3% |
| Dati storici | 2021-2022 |
| Periodo di previsione | 2024-2031 |
| Segmenti coperti | Per progettazione dello studio
|
| Regioni e paesi coperti | Europa
|
| Leader di mercato e profili aziendali chiave |
|
Tra i principali attori del mercato figurano, tra gli altri, QVIA Holdings Inc, Parexel International Corp, IXICO Plc, Charles River Laboratories International Inc, ICON Plc, WuXi AppTec Co Ltd, SGS SA, Syneos Health Inc, Thermo Fisher Scientific Inc, Laboratory Corp of America Holdings, CliniRx Research Private Limited, Caidya, Oracle Corp, Medpace Holdings Inc e SIRO Clinpharm Pvt Ltd. Questi attori stanno adottando diverse strategie, come espansione, innovazione di prodotto e fusioni e acquisizioni, per offrire prodotti innovativi ai propri consumatori e aumentare la propria quota di mercato.
Per la raccolta e l'analisi dei dati presentati nel presente rapporto è stata seguita la seguente metodologia:
Il processo di ricerca inizia con una ricerca secondaria completa, che utilizza fonti interne ed esterne per raccogliere dati qualitativi e quantitativi per ciascun mercato. Le fonti di ricerca secondaria comunemente utilizzate includono, a titolo esemplificativo ma non esaustivo:
Nota: tutti i dati finanziari inclusi nella sezione "Profili aziendali" sono stati standardizzati in USD. Per le aziende che redigono i bilanci in altre valute, i dati sono stati convertiti in USD utilizzando i tassi di cambio dell'anno corrispondente.
Ogni anno, Insight Partners conduce un numero significativo di interviste primarie con stakeholder ed esperti del settore per convalidare l'analisi dei dati e ottenere informazioni preziose. Queste interviste di ricerca sono progettate per:
La ricerca primaria viene condotta tramite interazioni via e-mail e interviste telefoniche, comprendendo vari mercati, categorie, segmenti e sottosegmenti in diverse regioni. I partecipanti includono in genere:
Il mercato europeo degli studi clinici è valutato a 12.286,73 milioni di dollari nel 2023 e si prevede che raggiungerà i 20.056,53 milioni di dollari entro il 2031.
Secondo il nostro rapporto Europe Clinical Trials Market, il mercato ha un valore stimato di 12.286,73 milioni di dollari nel 2023, con una previsione di raggiungere i 20.056,53 milioni di dollari entro il 2031. Ciò si traduce in un CAGR di circa il 6,3% nel periodo di previsione.
Il rapporto sul mercato degli studi clinici in Europa in genere copre questi segmenti chiave:
Il periodo storico, l'anno base e il periodo di previsione possono variare leggermente a seconda dello specifico rapporto di ricerca di mercato. Tuttavia, per il rapporto sul mercato degli studi clinici in Europa:
Periodo storico: 2021-2022Anno base: 2023Periodo di previsione: 2024-2031Il mercato europeo degli studi clinici è popolato da diversi attori chiave, ognuno dei quali contribuisce alla sua crescita e innovazione. Tra i principali attori figurano:
QVIA Holdings IncParexel International CorpIXICO PlcCharles River Laboratories International IncICON PlcWuXi AppTec Co LtdSGS SASyneos Health IncThermo Fisher Scientific IncLaboratory Corp of America HoldingsCliniRx Research Private LimitedCaidyaOracle CorpMedpace Holdings IncSIRO Clinpharm Pvt LtdQVIA Holdings IncIl rapporto sul mercato degli studi clinici in Europa è utile per diverse parti interessate, tra cui:
In sostanza, chiunque sia coinvolto o stia prendendo in considerazione un coinvolgimento nella catena del valore del mercato europeo degli studi clinici può trarre vantaggio dalle informazioni contenute in un rapporto di mercato completo.